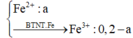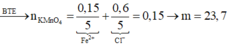cho 11,2 g CaO tác dụng với dung dịch có chứa 39,2 g H2SO4.phản ứng xảy ra thu được CaSO4 và H2O.tính khối lượng các chất còn lại trong phản ứng hoá học trên

Những câu hỏi liên quan
Câu 11. Cho 11,2 g CaO tác dụng với dung dịch có chứa 39,2 g H2SO4. Tính khối lượng các chất còn lại trong phản ứng hóa học trên (không tính khối lượng nước)Câu 12. Đốt cháy 6,4 g lưu huỳnh bằng 11,2 lít khí O2 (đktc) thu được sản phẩm là SO2. Tính thể tích của các khí thu được sau phản ứng hóa học trên ở đktcCâu 13. Đốt cháy 4,8 g cacbon bằng 6,72 lít khí oxi thu được sản phẩm sau phản ứng là CO2. Tìm khối lượng chất còn dư và thể tích khí CO2 thu đượcCâu 14. Cho 20,8 g BaCl2 tác dụng với dung...
Đọc tiếp
Câu 11. Cho 11,2 g CaO tác dụng với dung dịch có chứa 39,2 g H2SO4. Tính khối lượng các chất còn lại trong phản ứng hóa học trên (không tính khối lượng nước)
Câu 12. Đốt cháy 6,4 g lưu huỳnh bằng 11,2 lít khí O2 (đktc) thu được sản phẩm là SO2. Tính thể tích của các khí thu được sau phản ứng hóa học trên ở đktc
Câu 13. Đốt cháy 4,8 g cacbon bằng 6,72 lít khí oxi thu được sản phẩm sau phản ứng là CO2. Tìm khối lượng chất còn dư và thể tích khí CO2 thu được
Câu 14. Cho 20,8 g BaCl2 tác dụng với dung dịch chứa 9,8 g H2SO4. Tính khối lượng các chất thu được sau phản ứng.
Câu 15. Cho 20 g CuO tác dụng với dung dịch chứa 18,25 g HCl. Tính khối lượng các chất thu được sau phản ứng.
Câu 11:
\(n_{CaO}=\dfrac{11,2}{56}=0,2\left(mol\right);n_{H_2SO_4}=\dfrac{39,2}{98}=0,4\left(mol\right)\)
PTHH: \(CaO+H_2SO_4\rightarrow CaSO_4+H_2O\)
Ban đầu: 0,2 0,4 0,2
Sau pư: 0 0,2 0,2
`=>`\(\left\{{}\begin{matrix}m_{H_2SO_4}=0,2.98=19,6\left(g\right)\\m_{CaSO_4}=0,2.136=27,2\left(g\right)\end{matrix}\right.\)
Câu 12:
\(n_S=\dfrac{6,4}{32}=0,2\left(mol\right);n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: \(S+O_2\xrightarrow[]{t^o}SO_2\)
Ban đầu: 0,2 0,5
Sau pư: 0 0,3 0,2
`=>`\(\left\{{}\begin{matrix}V_{O_2}=0,3.22,4=6,72\left(l\right)\\V_{SO_2}=0,2.22,4=4,48\left(l\right)\end{matrix}\right.\)
Câu 13:
\(n_C=\dfrac{4,8}{12}=0,4\left(mol\right);n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: \(C+O_2\xrightarrow[]{t^o}CO_2\)
Ban đầu: 0,4 0,3
Sau pư: 0,1 0 0,3
`=>`\(\left\{{}\begin{matrix}m_{C\left(d\text{ư}\right)}=0,1.12=1,2\left(g\right)\\V_{CO_2}=0,3.22,4=6,72\left(l\right)\end{matrix}\right.\)
Câu 14:
\(n_{BaCl_2}=\dfrac{20,8}{208}=0,1\left(mol\right);n_{H_2SO_4}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
PTHH: \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
Ban đầu: 0,1 0,1
Sau pư: 0 0 0,1 0,2
`=>`\(\left\{{}\begin{matrix}m_{BaSO_4}=0,1.233=23,3\left(g\right)\\m_{HCl}=0,2.36,5=7,3\left(g\right)\end{matrix}\right.\)
Câu 15:
\(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right);n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
PTHH: \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
Ban đầu: 0,25 0,5
Sau pư: 0 0 0,25
`=>`\(m_{CuCl_2}=0,25.135=33,75\left(g\right)\)
Đúng 2
Bình luận (0)
Đốt một mẫu than chì chứa tạp chất lưu huỳnh trong oxi. Cho hỗn hợp khí thoát ra tác dụng với lượng dư dung dịch brom, thấy có 0,32 g brom đã phản ứng. Cho khí thoát ra khỏi dung dịch brom tác dụng với lượng dư nước vôi trong, thu được 10,00 g kết tủa.1. Viết phương trình hoá học của các phản ứng xảy ra.2. Xác định phần trăm khối lượng của cacbon trong mẫu than chì.
Đọc tiếp
Đốt một mẫu than chì chứa tạp chất lưu huỳnh trong oxi. Cho hỗn hợp khí thoát ra tác dụng với lượng dư dung dịch brom, thấy có 0,32 g brom đã phản ứng. Cho khí thoát ra khỏi dung dịch brom tác dụng với lượng dư nước vôi trong, thu được 10,00 g kết tủa.
1. Viết phương trình hoá học của các phản ứng xảy ra.
2. Xác định phần trăm khối lượng của cacbon trong mẫu than chì.
Thực hiện phản ứng nhiệt nhôm hỗn hợp bột X (gồm Al và một oxit sắt) sau phản ứng thu được 92,35 gam chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư, phản ứng xong vẫn còn phần không tan Z và thu được 8,4 lít khí E (đktc). Cho 1/4 lượng chất Z tan hoàn toàn trong dung dịch H2SO4 đặc nóng cần vừa đủ 60 gam H2SO4 98%. Biết các phản ứng xảy ra hoàn toàn . Khối lượng Al2O3 tạo thành có chứa trong chất rắn Y là: 98%. Biết các phản ứng xảy ra hoàn toàn. Khối lượng Al2O3 tạo thành có chứa trong chất r...
Đọc tiếp
Thực hiện phản ứng nhiệt nhôm hỗn hợp bột X (gồm Al và một oxit sắt) sau phản ứng thu được 92,35 gam chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư, phản ứng xong vẫn còn phần không tan Z và thu được 8,4 lít khí E (đktc). Cho 1/4 lượng chất Z tan hoàn toàn trong dung dịch H2SO4 đặc nóng cần vừa đủ 60 gam H2SO4 98%. Biết các phản ứng xảy ra hoàn toàn . Khối lượng Al2O3 tạo thành có chứa trong chất rắn Y là: 98%. Biết các phản ứng xảy ra hoàn toàn. Khối lượng Al2O3 tạo thành có chứa trong chất rắn Y là
A. 38,08 gam
B. 40,8 gam
C. 24,48 gam
D. 48,96 gam
Do khi phản ứng với NaOH tạo khí nên Al dư, oxit sắt hết .
Z là Fe.
2Fe+ 6H2SO4 → Fe2(SO4)3 + 3SO2 + 6H2O
=> n Fe = 0,2 mol => n Fe (Z)= 0,8 mol
Lại có n H2 = 0,375 mol
=> nAl (Z) =0,25 mol
=> m Al2O3(Z)= 92,35 – 56.0,8 – 0,25.27 =40,8 g =>B
Đúng 0
Bình luận (0)
. Cho 20 g hỗn hợpX gồm CuO, Cu, Ag tác dụng vừa đủ với dung dịch chứa 3,92 gam H2SO4 sau phản ứng thu được dung dịch B và 4 gam chất rắn C. Viết phương trình hoá học và tính khối lượng oxit có trong hỗn hợp X
Bài 2. Cho 15,8 g gam hỗn hợp X gồm Fe và Al2O3 tác dụng vừa đủ với 200 ml dung dịch H2SO4 thu được 2,24 lít khí (ở điều kiện tiêu chuẩn). a) Viết các phương trình hoá học của phản ứng xảy ra. b) Tính khối lượng mỗi chất trong hỗn hợp X. c) Tính nồng độ mol của dung dịch H2SO4 đã dùng. Cứu cần gấp
\(n_{H2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
a) \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
b) \(n_{Fe}=n_{H2}=n_{H2SO4}=0,1\left(mol\right)\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
\(\Rightarrow m_{Al2O3}=15,8-5,6=10,2\left(g\right)\)
c) Ta có : \(n_{Al2O3}=\dfrac{10,2}{102}=0,1\left(mol\right)\Rightarrow n_{H2SO4}=3n_{Al2O3}=0,3\left(mol\right)\)
\(C_{MddH2SO4}=\dfrac{0,1+0,3}{0,2}=2M\)
Đúng 4
Bình luận (0)
Cho 10g MgO tác dụng với 400g dung dịch H2SO4 49% a. Viết PTHH của phản ứng xảy ra b. Tính khối lượng muối thu được sau phản ứng c. Tính nồng độ phần trăm các chất có trong dung dịch sau phản ứng
PTHH: \(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{MgO}=\dfrac{10}{40}=0,25\left(mol\right)\\n_{H_2SO_4}=\dfrac{400\cdot49\%}{98}=2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Axit còn dư, MgO p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{MgSO_4}=0,25\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=1,75\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{MgSO_4}=0,25\cdot120=30\left(g\right)\\m_{H_2SO_4\left(dư\right)}=1,75\cdot98=171,5\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd\left(sau.p/ứ\right)}=m_{MgO}+m_{ddH_2SO_4}=410\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgSO_4}=\dfrac{30}{410}\cdot100\%\approx7,31\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{171,5}{410}\cdot100\%\approx41,83\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Số mol của magie oxit
nMgO = \(\dfrac{m_{MgO}}{M_{MgO}}=\dfrac{10}{40}=0,25\left(mol\right)\)
Khối lượng của axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{ct}=\dfrac{C.m_{dd}}{100}=\dfrac{49.400}{100}=196\left(g\right)\)
Số mol của axit sunfuric
nH2SO4= \(\dfrac{m_{H2SO4}}{M_{H2So4}}=\dfrac{196}{98}=2\left(mol\right)\)
a)Pt : MgO + H2SO4 → MgSO4 + H2O\(|\)
1 1 1 1
0,25 2 0,25
b) Lập tỉ số so sánh : \(\dfrac{0,25}{1}< \dfrac{2}{1}\)
⇒ MgO phản ứng hết , H2SO4 dư
⇒ Tính toán dựa vào số mol MgO
Số mol của muối magie sunfat
nMgSO4 = \(\dfrac{0,25.1}{1}=0,25\left(mol\right)\)
Khối lượng của muối magie sunfat
mMgSO4 = nMgSO4 . MMgSO4
= 0,25 . 120
= 30 (g)
Số mol dư của dung dịch axit sunfuric
ndư = nban đầu - nmol
= 2 - (0,25 . 1)
= 1,75 (g)
Khối lượng dư của dung dịch axit sunfuric
mdư = ndư . MH2SO4
= 1,75 . 98
= 171,5 (g)
Khối lượng của dung dịch sau phản ứng
mdung dịch sau phản ứng = mMgO + mH2SO4
= 10 + 400
= 410 (g)
Nồng độ phần trăm của dung dịch magie sunfat
C0/0MgSO4= \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{30.100}{410}=7,32\)0/0
Nồng độ phần trăm của dung dịch axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{171,5.100}{410}=41,83\)0/0
Chúc bạn học tốt
Đúng 0
Bình luận (0)
Cho 26 g Zn tác dụng với 500ml dung dịch H2SO4 loãng 1M (biết khối lượng riêng dung dịch D=1,12 g/ml) thu được ZnSO4 và khí hidro thoát ra
a,viết phương trình phản ứng xảy ra
b,tính thể tích khí hidro thoát ra
c,tính khối lượng ZnSO4 tạo thành
d, tính C% của các chất trong dung dịch thu được sau phản ứng kết thúc
nZn=0,4mol
nH2SO4=0,5mol
PTHH: Zn+H2SO4=>ZnSO4+H2
0,4:0,5=> nH2SO4 dư theo nZn
p/ư: 0,4->0,4----->0m4---->0,4
=> VH2=0,4.22,4=8,96ml
b) mZnSO4 tạo thành : m=0,4.161=64,4g
c) ta có mđ H2SO4=1,12.500=560g
mddZnSO4=26+560-0,4.2=585,2g
=> C%(ZnSO4)=64,4:585,2.100=11%
Đúng 0
Bình luận (1)
Cho Al tác dụng với dung dịch H2SO4 loãng thì xảy ra phản ứng hoá học theo sơ đồ sau: Al + H2SO4 → Al2(SO4)3 + H2
Cho biết sau phản ứng thu được 74,37 lít khí H2 (ở 250C và 1 bar). Hãy tính:
a. Khối lượng Al đã tham gia phản ứng.
b. Khối lượng acid H2SO4 đã tham gia phản ứng.
mg giúp mình vs ạ
Đọc tiếp
Cho Al tác dụng với dung dịch H2SO4 loãng thì xảy ra phản ứng hoá học theo sơ đồ sau: Al + H2SO4 → Al2(SO4)3 + H2
Cho biết sau phản ứng thu được 74,37 lít khí H2 (ở 250C và 1 bar). Hãy tính:
a. Khối lượng Al đã tham gia phản ứng.
b. Khối lượng acid H2SO4 đã tham gia phản ứng.
mg giúp mình vs ạ
Ta có: \(n_{H_2}=\dfrac{74,37}{24,79}=3\left(mol\right)\)
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
a, \(n_{Al}=\dfrac{2}{3}n_{H_2}=2\left(mol\right)\)
\(\Rightarrow m_{Al}=2.27=54\left(g\right)\)
b, \(n_{H_2SO_4}=n_{H_2}=3\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=3.98=294\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 11,2 gam Fe vào 300 ml dung dịch chứa (HNO3 0,5M và HCl 2M) thu được khí NO duy nhất và dung dịch X. Cho dung dịch X tác dụng với lượng dư dung dịch KMnO4/H2SO4 loãng. Biết các phản ứng xảy ra hoàn toàn. Tính khối lượng KMnO4 đã bị khử. A. 4,71 gam. B. 23,70 gam. C. 18,96 gam. D. 20,14 gam.
Đọc tiếp
Cho 11,2 gam Fe vào 300 ml dung dịch chứa (HNO3 0,5M và HCl 2M) thu được khí NO duy nhất và dung dịch X. Cho dung dịch X tác dụng với lượng dư dung dịch KMnO4/H2SO4 loãng. Biết các phản ứng xảy ra hoàn toàn. Tính khối lượng KMnO4 đã bị khử.
A. 4,71 gam.
B. 23,70 gam.
C. 18,96 gam.
D. 20,14 gam.